
第一作者:耿立珊
通讯作者:麦立强&孟甲申
通讯单位:武汉理工大学
DOI:10.1021/acsenergylett.6c00406
感谢武汉理工大学麦立强团队(第一作者:耿立珊)校稿!
成果简介
本综述全面总结了锌卤素液流电池(ZHFBs)电解液化学领域的最新进展,重点涵盖五个关键方面:电解液组成、溶剂化结构、锌沉积电化学、卤素反应行为及pH效应。文章系统分析了影响活性离子(Zn²⁺和卤化物)反应动力学的优化机制、调控锌沉积的电位与界面反应,以及卤素物种的氧化还原路径。此外,本文还探讨了当前面临的挑战,并提出了ZHFBs电解液开发的未来研究方向。
背景分析
ZHFBs的实际应用受到诸多关键挑战的严重阻碍,例如锌枝晶的形成和多卤化物穿梭现象,两者均与电解液化学特性密切相关。过去几十年间,大量研究致力于解决这些问题,凸显出亟需对有效的优化策略进行全面而深入的理解。然而,现有的关于锌基电池的综述通常提供广泛的概述,涵盖电极材料的改进、电解液和隔膜的优化,或多种电池系统,包括Zn−Br电池、Zn−I电池、Zn−空气电池以及锌离子电池。仍然明显缺乏的是对ZHFB特有的电解液化学进行系统和专门的分析,特别是在阐明电解液成分、溶剂化结构、界面电化学行为之间的复杂相互作用及其对电池性能的集体影响方面。
图文解析
1.锌卤素液流电池中的电解液问题
ZHFBs的实际应用受到循环寿命有限、CE低以及稳定性差等问题的制约,根本原因在于传统水基电解液的固有特性,而非单纯的工程难题。电解液的化学性质(包括其组成、溶剂化结构以及热力学和动力学特性)决定了电化学性能,也是这些失效模式的主要根源。
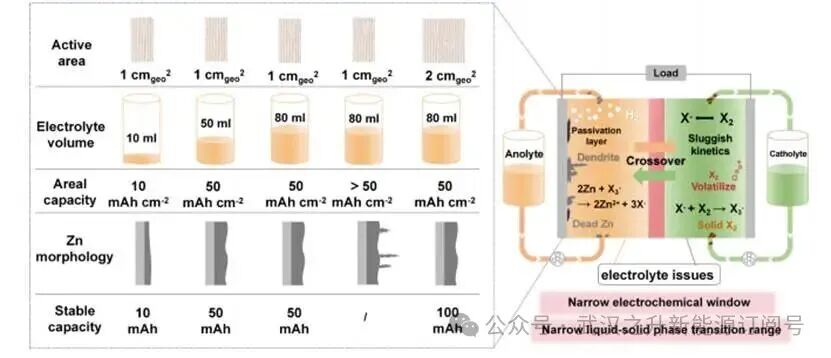
图1.ZHFBs在传统电解液中的应用挑战
1.1锌电镀/剥离故障的电解液原因分析
Zn²⁺/Zn的还原电位(−0.76V vs SHE)接近水和质子的还原电位,使得HER成为不可避免的寄生副反应。HER不仅消耗电荷,降低锌电镀/剥离的CE,还会局部升高pH。pH的升高促进了电极表面氢氧化锌和氧化钝化层的形成与沉淀。此外,即使没有外加电流,沉积的锌层也会通过反应(Zn+2H⁺→Zn²⁺+H₂)持续发生化学腐蚀,导致ZHFBs自放电。
锌电镀的形貌由离子传输和界面反应动力学决定。在传统的水性电解液中,Zn²⁺以六水合络合物[Zn-(H2O)₆]²⁺的形式存在。[Zn(H2O)₆]²⁺的去溶剂化过程会形成能量势垒,导致非均匀成核和尖端效应,从而促进枝晶生长。这种现象在高面容量下尤为显著。随着锌沉积厚度的增加,界面对Zn²⁺的需求超过了离子从本体电解液中扩散的速率,从而引发严重的浓差极化。当沉积过程转为扩散控制时,由于扩散距离缩短,突起区域的离子通量增强,从而在循环中加速局部枝晶生长,表明电解液化学是锌电极不稳定性的根本原因。
1.2卤素转化失败的电解液原因分析
卤素转化反应的失败主要归因于四个由电解液主导的挑战。首先,穿梭效应源于可溶性元素卤素(X2)和多卤化物(X3)−在隔膜中的扩散,导致沉积锌发生寄生氧化并快速自放电(Zn+X2→Zn2++2X−;Zn+X3−→Zn2++3X−)。这种交叉现象由这些物质的渗透性决定,而渗透性受络合剂效能及电解液物理性质的影响。其次,I−/I2/I3−卤素氧化还原对所固有的电子转移和相变会导致反应动力学缓慢和高极化现象。反应速率受电解液因素控制,包括局部卤化物浓度、卤素间键合强度及质量传输。第三,生成卤素(尤其是溴和氯气)的挥发性和高腐蚀性会导致活性材料损失,并带来显著的安全与组件劣化风险。最后,卤素物种的反应路径和稳定性高度依赖pH值。例如,在碱性介质中,元素溴可歧化为溴化物和次卤酸盐,导致不可逆的容量损失。
1.3电解液的固有局限性
除了特定电极反应外,ZHFBs的整体性能从根本上受限于传统水性电解液的固有局限性。两个普遍且与系统无关的挑战是:狭窄的电化学稳定性窗口(ESW)以及有限的液相温度范围。工作电压被限制在水的热力学ESW之内,对不同电对施加了严格的约束。体系的工作电压均达到或超过此实际极限,在充电过程中会在正极引发OER。OER会与卤素氧化反应竞争,降低CE、消耗活性材料,并引发有害的电解液变化,从而威胁长期稳定性。因此,电压上限不仅代表了能量密度的限制,更是长期运行稳定性的根本障碍。
枝晶形成、析氢、卤素穿梭、腐蚀以及pH敏感性等挑战在静态和ZHFBs中普遍存在,因为这些现象源于Zn²⁺/Zn及卤素化学的固有特性。然而,由于独特的流动架构,这些挑战的表现形式及缓解要求存在显著差异。连续电解液循环以及功率与能量的解耦提出了不同的要求:液流电池需要严格均一的反应环境,因为任何沉淀物或凝胶都会堵塞电极、流动通道和泵;它们还需要主动的、系统级的pH管理(而非局部界面缓冲);对材料兼容性要求更宽泛(因腐蚀性电解液会接触泵、管路、密封件和储罐);以及需要针对数千次循环而非数百次循环的长期循环稳定性。这些差异表明ZHFBs的电解液设计必须超越静态电池策略,将化学功能特性与流体动力学兼容性、动态过程控制及多组分系统集成相结合,以实现实用且可扩展的应用。
2.电解液设计策略
为克服ZHFBs的基本挑战,先进的电解液设计策略已成为关键解决方案。主要侧重于分子层面的设计,以精确调控块体电解液的特性,包括溶剂化结构、锌界面反应、卤素氧化还原反应行为以及pH环境。关键在于,四个方面并非相互独立:Zn²⁺的溶剂化结构直接决定了其界面传输和HER活性,从而调控锌界面反应,进而影响局部pH;反之,pH强烈影响卤素的形态分布和反应路径,而卤离子本身也可能参与Zn²⁺的溶剂化过程,且卤离子的溶剂化结构同样会影响卤素反应的动力学。
2.1电解液组成
电解液调节的基础步骤是对核心成分的合理选择,包括对活性溶质、辅助盐类及功能性添加剂的审慎挑选(图2)。成分的选择直接决定了溶剂化结构、反应行为及pH值。
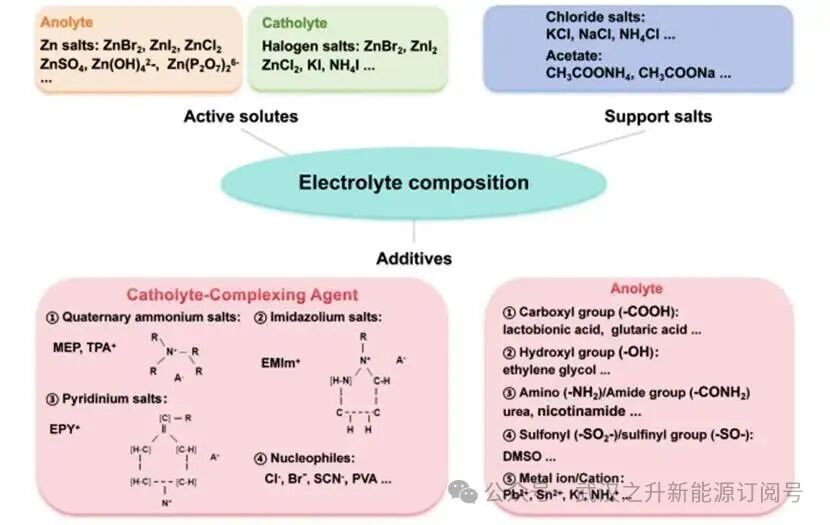
图2.ZHFBs的电解液组成
2.1.1活性溶质
活性溶质是电解液的核心,为能量存储提供电活性物质。对于阳极电解液而言,首要要求是Zn2+的来源;而对于阴极电解液,活性物质则是卤素离子(X⁻)。锌卤化物盐(例如ZnBr2、ZnCl2)是最常用的选择,可同时作为锌阳极电解液和卤素阴极电解液的来源。此外,先进的配置方案可采用具有不同活性溶质的独立阳极电解液和阴极电解液,以分别优化各电极的反应。例如,硫酸锌被选作阳极电解液的活性溶质,而KI、碘化铵或溴化钾则作为阴极电解液的活性溶质,其中硫酸锌已在静态锌离子电池中得到广泛研究,而K+或NH4+可影响多碘化物的溶解度及电化学双电层的形成。此外,在碱性电解液中,锌源可以复合阴离子形式存在,如Zn(OH)42-或Zn(P2O7)26-,会显著改变沉积机制,尤其是锌沉积电位。
活性溶质的浓度是ZHFBs的关键参数。提高活性溶质浓度会增加载流子数量,从而提升电池容量。然而,当浓度超过某个临界点时,由于离子-离子及离子-溶剂相互作用增强,会导致电解液粘度升高,会降低电解液的离子电导率。此外,高浓度电解液(尤其是“盐水溶液”电解液)会降低水活度,但同时也可能加速腐蚀;当浓度接近饱和极限时,运行过程中还存在盐结晶的风险。
2.1.2辅助盐类
支撑盐由电化学惰性的阳离子和阴离子组成,例如氯化钾、氯化钠、氯化铵、CH3COONH4和CH3COONa。主要功能是通过增加电荷载流子的总浓度来提高离子导电性。尤其在高浓度卤化锌溶液中,支撑离子可提供替代的导电路径,以减轻由粘稠卤化锌基质引起的导电性损失。然而,会导致支撑离子浓度过高并增加溶液粘度。
除了影响整体传输特性外,支撑盐还能调节界面电化学反应及离子-溶剂相互作用。支撑盐中的阳离子种类通过界面效应显著影响锌沉积的形貌。例如,NH4+表现出独特行为,会优先吸附在锌沉积层上。这种吸附会产生一个阳离子屏蔽层,使界面电场均匀化,促进横向锌生长并抑制枝晶形成。此外,在支撑盐的碱金属阳离子中,促进锌均匀沉积的效果遵循K+>Na+>Li+的趋势,与其水合半径和吸附能密切相关。水合能力最弱的K+能轻易接近电极界面,在双电层中形成致密结构并使电场均匀化,有助于实现均匀成核和致密的锌沉积;而水合程度较高的Li+则会形成弥散层,促进枝晶生长。阴离子组分(通常为Cl⁻)在调节Zn2+的溶剂化结构方面发挥着互补作用:Cl–可置换水分子进入Zn2+的初级溶剂化层,形成接触离子对,从而降低电极界面的水活度并提高析氢的过电位。此外,溶剂化结构的改变还会影响Zn2+的脱水动力学,进而调控其成核行为。
2.1.3电解液添加剂
作为功能性组分,添加剂能够选择性地影响界面反应、溶剂化结构及质量传输,从而高效地解决枝晶形成和卤素穿梭两种核心失效模式。在阴极电解液中,络合剂主要被添加用于抑制卤素穿梭现象,络合剂可分为四类:季铵盐、咪唑鎓盐、吡啶鎓盐和亲核试剂。常见的季铵盐包括MEP(N-甲基-N-乙基吡咯烷溴化物)和TPABr(四丙基溴化铵);典型的咪唑鎓盐是EMImBr(1-乙基-3-甲基咪唑鎓溴化物);而常见的吡啶鎓盐则是EPYBr(1-乙基吡啶鎓溴化物)。所有络合剂均能通过静电相互作用与多卤化物阴离子结合,随后因疏水相互作用形成致密且不溶于水的液相,它们的络合能力与其分子结构密切相关。亲核试剂通常会将平衡反应(X⁻+X₂⇌X₃⁻)向反应物方向移动,从而抑制穿梭现象,尤其适用于Zn⁻/I⁻电池。Cl⁻、Br⁻、SCN⁻和PVA可分别与I₂结合,形成I₂Cl⁻、I₂Br⁻、I₂SCN⁻和I₂-PVA液相或凝胶络合物,从而抑制I₃⁻穿梭的形成。在阳极电解液中,添加剂旨在通过修饰电极-电解液界面来实现均匀的锌沉积,根据官能团可分为以下五类:(i)羧基(-COOH)。乳糖酸和戊二酸等分子会强烈吸附在锌沉积层上,从而增加成核位点数量并形成更细粒度的沉积物。此外,它们还能与本体电解液中的Zn²⁺发生弱配位作用,微妙地改变溶剂化结构;(ii)羟基(−OH)。乙二醇等添加剂可通过与水分子形成氢键破坏水网络,从而提高HER的过电位;(iii)NH2/−CONH₂。这些基团可吸附在锌表面并参与Zn²⁺的溶剂化壳层,从而改变沉积动力学;(IV)−SO₂⁻/−SO⁻。3,3′-联吡啶磺酸盐和二甲基亚砜(DMSO)等化合物是高效的水分子调节剂。强极性使其能有效与水分子竞争Zn²⁺周围的配位位点,形成贫水的内部溶剂化壳层以抑制HER;(V)金属离子/阳离子。无机添加剂可通过优先沉积或吸附发挥作用。例如,Pb²⁺和Sn²⁺具有较高的HER过电位,相较于Zn²⁺沉积会优先沉积,形成保护层。
3.溶剂化结构设计
基于特定的电解液组成,溶剂化结构设计是将整体性能转化为所需界面行为的关键第一步。溶剂化结构决定了离子传输动力学、界面稳定性以及副反应等关键过程。合理设计溶剂化结构可显著提升ZHFBs的循环寿命、EE和容量。
3.1溶剂化结构的形成机制
电解液中中心离子的溶剂化结构是一个分层结构,主要由一级溶剂化层(内层球壳)和二级溶剂化层(外层球壳)组成。该溶剂化结构的形成是通过分子间力的复杂相互作用实现的。最基础的作用力包括配位键(路易斯酸碱相互作用)、氢键以及偶极-偶极相互作用。这些作用力的相对强度及其协同效应共同决定了溶剂化结构的最终空间排列、稳定性及动态特性。
配位键是形成初级溶剂化壳层的主要且最强的相互作用,直接影响去溶剂化能垒。这种相互作用本质上是一种路易斯酸碱反应:Zn²⁺作为电子对受体(路易斯酸),而溶剂分子或阴离子则作为电子对供体(路易斯碱)(图3a)。Zn²⁺-溶剂配位强度主要受供体数(DN)和溶剂极化率的影响。供体数是路易斯碱性的定量指标,反映了溶剂向中心Zn²⁺提供电子对的能力。与水等较弱供体相比,具有高DN值的溶剂(如二甲基亚砜)能与Zn²⁺形成更强、更稳定的配位键。同时,通过电子云畸变难易度量化的极化率会影响键的共价特性:高极化率溶剂能与Zn²⁺更有效地发生轨道重叠,从而增强相互作用。对于Zn²⁺与阴离子间的配位强度,阴离子的电荷越高、半径越小,其电荷密度越大,静电吸引力就越强(例如:SO₄²⁻>Ac⁻>NO3–>Cl⁻>BF4–>ClO₄⁻>CF₃SO₃⁻>ClOTFSI−)。然而,对于半径较大的阴离子,必须考虑其极化率,即电子云发生畸变的难易程度。高极化率的阴离子会引发额外的极化相互作用或电荷转移,从而增强整体配位强度。主要溶剂化层内的强配位相互作用可增强结构稳定性;同时也会提高去溶剂化能垒。
HBs主导着二级溶剂化层及扩展的溶剂网络。氢键通常形成于溶剂分子之间以及溶剂与阴离子之间,影响离子的迁移率及电解液的整体粘度。更为关键的是,氢键也可存在于一级溶剂化层与外部溶剂分子之间,介导溶剂分子间的交换。氢键具有部分共价特性,其本质是氢原子(作为氢键供体D)与另一个带有孤对电子的高电负性原子(氢键受体A)之间产生的静电吸引作用。氢键的通用表示为D−H···A(图3b)。氢键的强度通常强于范德华力,但弱于配位键;其强度取决于D−H键的极性及氢键受体A的电子密度。此外,较短的H···A距离也会增强氢键作用,当D−H···A角接近180°时,由于轨道重叠与静电作用达到最佳状态,氢键强度达到最大。溶剂之间或溶剂与离子之间的强氢键可限制溶剂的活性,或稳定溶剂化离子。
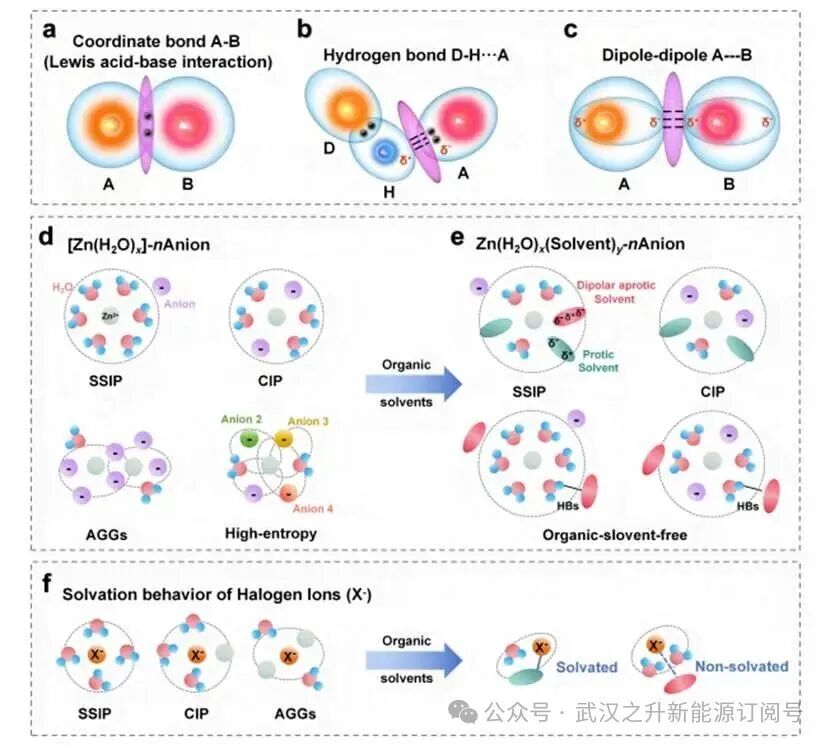
图3.溶剂化结构设计
偶极-偶极相互作用对于极性非质子溶剂对离子的溶剂化过程以及溶剂化结构的整体稳定性至关重要。这些相互作用本质上是具有永久偶极矩的分子之间产生的普遍静电作用力(图3c)。极性溶剂分子本身具有永久偶极矩;当离子引入时,离子产生的电场会对溶剂分子的偶极矩施加扭矩,使其重新定向,使相反电荷朝向离子排列。该相互作用的强度与参与作用的偶极矩之积成正比,与它们之间距离的立方成反比,其强度弱于配位作用和氢键。极性溶剂与离子之间的强偶极-偶极相互作用可促进盐的解离,从而削弱阳离子与阴离子之间的相互作用,进而提高游离离子的浓度。
不同离子配对构型,溶剂分离离子对(SSIP)、接触离子对(CIP)和离子聚集体(AGGs)的形成,由阳离子-溶剂、阳离子-阴离子以及溶剂-溶剂之间的竞争性平衡所决定(图3d)。在SSIP中,离子被至少一个溶剂层完全溶剂化和分离,其中强烈的阳离子-溶剂配位有效地屏蔽了直接的库仑引力。当阴离子直接与阳离子配位并进入其初级溶剂化层时,即形成CIP(阴离子-阳离子配位结构)。此过程发生在离子对之间的路易斯酸-碱相互作用与库仑吸引力共同克服了被置换溶剂分子的结合能时。这种阴离子对溶剂的取代作用会进一步发展为AGG(阴离子-阳离子桥接结构),其中阴离子桥接多个阳离子,形成以强离子-离子相互作用为主导的簇状结构。
3.2.Zn2+的溶剂化结构
在传统的水性电解液中,尤其是在传统阳极电解液中,Zn²⁺主要以SSIP结构存在,具体而言是八面体[Zn(H2O)₆]²⁺配合物。这种溶剂化结构对锌负极的可逆性存在若干固有缺陷:(i)配位水分子的强极化作用会削弱O−H键,降低其还原电位并加剧HER;(ii)该配合物的高热力学稳定性导致较高的去溶剂化能垒,从而减缓Zn²⁺电荷转移动力学;(iii)电极-电解液界面处丰富的活性水会促进副反应及副产物的生成。
一种成熟的缓解这些问题的策略是通过调节溶剂化结构,将[Zn-(H2O)6]2+SSIP转化为CIP或AGGs(图3d),可以通过使用具有更高晶格能的锌盐、增加典型锌盐的浓度,或引入对Zn2+具有高亲和力的物种来实现。这些阴离子可部分置换初级溶剂化层中的水分子,形成CIP。在最终形成的混合溶剂化壳层[Zn-(H2O)6−x(阴离子)x]中,供电子阴离子减少了剩余配位水分子的电子缺陷。对模型溶剂化簇的计算研究表明这种修饰与LUMO能量的升高相关,该指标通常与配位水还原稳定性的改善相关。升高的LUMO能量被认为提高了H+还原的热力学能垒,从而有助于抑制HER。然而,在本体水性电解液中,HER抑制源于集体溶剂化效应(包括氢键网络的破坏、界面电双层的改变以及水活度的降低),而非仅由孤立的分子轨道变化引起。
随着离子配对作用增强,CIPs可进一步形成低水含量的AGG结构(例如ZnCl₄²⁻),从而降低整体水活度。然而,这种通过促进强阴离子配位的传统方法存在固有的权衡:虽然,能有效减少自由水含量,但会增加电解液粘度、略微降低离子电导率;对于高密度AGG而言,甚至可能提高Zn²⁺的去溶剂化能垒,从而抵消初始的动力学优势。更高的粘度会导致压降和泵送功增加,降低系统整体效率,对电网规模储能而言至关重要,因为CE直接决定其经济可行性。此外,高粘度还会减缓对流传质过程,加剧高电流密度下的浓度极化现象,部分抵消了降低水活度所带来的优势。
一项创新设计是高熵溶剂化策略,该策略灵感源自静态锌基电池的改性方法。该方法采用多种阴离子(通常包括多种卤化物离子)的混合物,以形成多样化的溶剂化环境。“高熵”这一术语在此概念上用于描述多阴离子混合物引入的成分复杂性和构型无序性的增强。这种结构阻止系统形成单一、主导且强结合的溶剂化结构(例如特定的多卤化物AGG),而是促进了各种接触离子对(CIPs)和阴离子聚集结构(AGGs)的定制化分布。例如,在含有0.02M ZnCl2、ZnBr2和ZnI2的2M ZnSO4碱性电解液中,不同卤化物离子之间的竞争性配位导致溶剂化区域主要由单卤化物CIPs主导。这种特定组成避免了通常与均质多卤化物AGG相关的过高去溶剂化能,从而优化了Zn²⁺传输动力学。该策略的主要考量在于电解液配方复杂性的增加。
另一项重要策略是引入有机溶剂添加剂。有机添加剂大致可分为质子性溶剂和极性非质子性溶剂,二者根据分子结构及与离子的相互作用,通过不同的机制调控溶剂化结构(图3e)。质子性溶剂含有可形成氢键的质子,既能作为路易斯碱与Zn²⁺配位,又能作为氢键供体与阴离子或其他水分子相互作用。而极性非质子性溶剂则通过结构中的外层负电荷、内层正电荷以及缺乏氢键供体,对阴离子产生非溶剂化效应。盐类中阳离子与阴离子的弱相互作用可促使质子性溶剂和极性非质子性溶剂共同参与Zn²⁺的一级溶剂化层,形成SSIP溶剂化层。当阳离子与阴离子相互作用较强时,质子性溶剂可嵌入Zn²⁺的一级溶剂化层,部分取代水分子形成CIP层。目前,Zn²⁺-有机溶剂策略是ZHFBs中最常用的溶剂化调控方法,能有效抑制水相关的副反应。然而,由于Zn²⁺与有机溶剂分子间存在强烈的配位作用,会导致Zn²⁺/Zn电荷转移动力学缓慢。
借鉴静态锌基电池的溶剂化修饰方法,构建不含有机溶剂的初级壳层弱溶剂化结构能够有效提升快速反应动力学,同时限制水的副反应。在弱离子配对条件下引入少量偶极非质子溶剂,可促使偶极非质子溶剂从Zn²⁺初级壳层中排除,从而形成无有机溶剂的溶剂化结构。此外,当阳离子和阴离子之间的相互作用相对较强时,偶极非质子溶剂更有可能被排除在Zn2+的内部配位范围之外,形成无有机溶剂的溶剂化环境。这种HER抑制机制主要由电解液驱动,根源在于溶剂化化学性质的改变。然而,电极界面处的实际HER速率还取决于氢中间体在锌表面的吸附能,而该吸附能又受电解液离子影响,进而取决于电双层的组成。因此,尽管溶剂化工程为缓解HER提供了基本的热力学基础,但观察到的动力学改善可能涉及电解液与电极之间的协同效应。
3.3卤素离子的溶剂化行为
卤素离子的溶剂化结构通过影响去溶剂化活化能和质量传输,对氧化动力学起着关键调控作用。然而,在ZHFBs中,卤素离子的溶剂化结构鲜有研究或报道。2X⁻→X²⁺+2e⁻的氧化反应始于溶剂化层的去溶剂化过程,该过程的能量势垒高度依赖于溶剂化强度。卤素离子固有的物理化学性质从根本上决定了其溶剂化倾向。在水环境中,具有高水合能的小离子(如Cl⁻)倾向于形成SSIP结构,被水分子紧密包裹;尽管这种强溶剂化作用赋予其良好的溶解性和高离子电导率,但也导致去溶剂化能垒较高,从而使氯气释放反应的动力学缓慢。相比之下,具有弱水合能的大离子(如I⁻)对溶液中的反离子(Zn²⁺)表现出更强的直接静电吸引力,易于形成CIPs,并通过卤素桥接进一步组装;此类结构使I⁻更易从配位层去溶剂化,从而表现出更快的氧化动力学。然而,相对松散的溶剂化环境也使其氧化产物(如I₃⁻)更具溶解性和流动性,引发显著的穿梭效应。Br−表现出中间行为,在低浓度时表现为SSIPs,而在高浓度时转变为CIPs。
随着有机溶剂、质子性溶剂(如醇类)以及偶极性非质子性溶剂(如DMSO)的引入,由于卤素离子分子结构的不同,它们在溶剂中形成了两种截然不同的微环境。质子性溶剂可通过离子-偶极相互作用和氢键来溶剂化卤素离子,而氢键的断裂会提高去溶剂化能垒。具有内部正电荷且缺乏氢键供体的偶极性非质子性溶剂与卤素离子的相互作用较弱,但能增强阳离子与卤素离子之间的相对吸引力,从而形成CIP/AGG结构。这种结构可降低去溶剂化能垒,但大离子对的形成可能导致扩散速率减慢。
此外,关于溶剂化结构的见解是在实际液流电池的动态环境中得出的。电解液的持续流动会影响电极界面处的局部浓度、所有物质的传质过程以及表面附近的剪切力。诸如流速和电极结构等参数决定了电解液在反应区的停留时间,会影响界面溶剂化层的稳态组成,进而影响Zn²⁺或X⁻离子去溶剂化的动力学过程。因此,优化ZHFBs的溶剂化结构时,必须综合考虑其在对流流动条件下的稳定性和功能表现,而不仅仅是静态条件下的性能。
3.4锌沉积的电极电位
锌沉积的电极电位直接反映了溶剂化结构特征。结合卤素反应电位,锌沉积电位决定了ZHFBs的理论电压值:锌沉积电位越负,ZHFBs的开路电压通常就越高。Zn²⁺的配位环境决定了锌沉积电位。对于锌沉积反应(Zn²⁺+2e⁻⇌Zn(s)),其平衡电极电位(E)由能斯特方程确定:
E=E0+RT/2F ln([Zn2+]free)
其中[Zn²⁺]free为Zn²⁺的自由活度(图4a)。在传统的水性阳极电解液中,Zn²⁺主要以[Zn(H2O)₆]²⁺的简单水合离子形式存在,使得在Zn²⁺浓度约为1mol/L时,[Zn²⁺]自由浓度接近该值。此时,锌沉积电位接近标准值−0.76V(相对于标准氢电极)。当阴离子或有机溶剂分子取代水合水分子,与Zn²⁺形成更强的配位键时,Zn²⁺的自由活度进一步降低,导致沉积电位变得更负。例如,在ZnCl2与K₄P₂O₇组成的体系中,Zn²⁺以Zn(P2O7)₂⁶⁻簇的形式存在。Zn²⁺与P2O7⁴⁻之间的强配位作用使锌沉积电位移至−1.08V(相对于标准氢电极),相应地将锌-碘液流电池的电压提升至1.61V。此外,在常见的碱性阳极电解液中,Zn离子与OH⁻形成更强的配位键,生成Zn(OH)₄²⁻,使锌沉积电位进一步负移至−1.21V(相对于标准氢电极),从而进一步提高电池电压(图4b)。
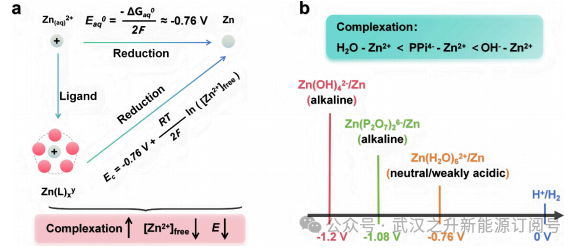
图4.锌沉积电位
尽管锌沉积电位的负向偏移会提高电池电压,但过负的沉积电位会导致锌沉积不稳定并加剧HER。更负的沉积电位会增强锌沉积的驱动力,从而显著增加成核位点的数量。因此,电极表面会瞬间生成大量细小的晶体核。然而,由于晶核形成速度过快,可能无法与基底形成牢固结合,导致锌沉积不稳定。在恒定pH条件下,HER的平衡电位保持不变。当强配体使锌沉积电位向更负值偏移时,必须采用更负的工作电位。根据Butler-Volmer方程,电极反应电流与过电位呈指数关系,因此由更负的锌沉积电位引起的过电位升高最终会加速HER反应动力学。
除了过电位论点之外,还需要认识到:经过修饰的溶剂化环境也可能影响调控HER的其他动力学参数。例如,Zn²⁺配位层的变化可通过改变电极界面处质子供体的可利用性和反应活性,从而影响HER的交换电流密度。此外,电极表面状态也可能受到强配位配体或有机添加剂存在的影响。在某些情况下,在显著改变的界面溶剂化条件下,主导的HER途径甚至可能发生变化。这些因素共同决定了净HER速率,而非仅由过电位决定。因此,尽管增加的过电位是主要驱动力,但要全面理解该过程,还需考虑溶剂化效应改变的交换电流密度与表面反应活性之间的协同作用。
3.4锌沉积过程中的界面电化学
锌电镀-剥离工艺的核心发生在负极与阳极电解液之间的固液界面。该界面并非理想的几何平面,而是具有复杂的电荷分布和离子排列结构,即所谓的电化学双电层(EDL)(图5a)。在传统阳极电解液中,内亥姆霍兹平面(IHP)通常由部分去溶剂化的阴离子和大量自由水分子组成,水分子源自[Zn(H2O)6]2+的水合离子。然而,在IHP中,电极表面高度活跃的自由水分子容易发生剧烈的HER,消耗电子和质子以生成H2和OH−。此外,生成的H2气泡以及OH−与Zn2+和阴离子结合形成的钝化副产物,会阻碍锌在K电极表面沉积的活性位点,会提高离子传输电阻,并导致锌沉积不均匀(图5a)。解决上述问题的关键对策是重建EDL,以排斥或替换IHP内的自由水分子(图5b)。常用方法包括:(i)引入具有强吸附能力的极性或两亲性分子,以替代IHP中的自由水;(ii)通过引入强吸附溶剂来构建Zn²⁺溶剂化鞘,从而置换溶剂化水,减少水向IHP的共转运。
从根本上说,锌沉积是一种相变过程:溶剂化的Zn²⁺在电极界面接受电子形成金属锌。在传统阳极电解液(浓度通常≤2M)中,该过程极易出现非均匀成核和生长现象,最终导致锌枝晶的形成。根本原因在于质量传输限制与界面反应动力学共同触发的自我强化恶性循环。首先,一旦沉积开始,界面处的Zn²⁺会被迅速消耗。由于Zn²⁺浓度有限且其迁移数较低,从主体阳极电解液中扩散的Zn²⁺无法补充被消耗的部分,从而产生显著的浓差极化。在由浓差极化驱动的扩散控制机制下,最初形成的核因其位置或尺寸优势,能够优先捕获并消耗周围绝大多数Zn²⁺,从而实现快速生长并形成初始突起。随后,稳定的[Zn(H2O)₆]²⁺溶剂化鞘层会因这些突起处增强的局部电场而发生去溶剂化,降低去溶剂化能垒并显著加速沉积动力学。此外,锌在突起处的沉积可能会形成新的突起,从而产生更强的局部电场,形成的恶性循环导致了尖端效应,而尖端效应的累积最终促使锌枝晶的形成(图5c)。
从根本上抑制枝晶生长的根本原因的两种主要策略是静电屏蔽和构建亲锌优先层。静电屏蔽方法采用比Zn²⁺还原电位更负的阳离子添加剂,阳离子在锌沉积电位下具有电化学惰性。在电场驱动下,会优先迁移并积聚在电场强度最高的突起区域,形成动态的带正电屏蔽层(图5d)。而亲锌层构建策略旨在优先形成具有高锌亲和力的界面层。亲锌层为Zn2+提供了许多低势垒成核位点,从初始阶段引导均匀的锌沉积。
该策略通常涉及两种方法(图5e):(i)引入比Zn²⁺具有更正还原电位的金属阳离子,使其能在电极上优先还原为金属纳米颗粒。这些金属纳米颗粒对后续沉积的锌具有强附着力且表面能均匀,显著降低了锌成核电位,并引导锌优先沉积在(002)晶面上;(ii)加入富含电负性O/N基官能团(如–羧基或–氨基)的亲锌有机添加剂。这些分子可吸附在锌负极表面形成稳定的吸附层,通过直接吸附或还原分解在电极表面形成亲锌层,作为亲锌位点引导均匀成核。
此外,尽管EDL调节策略、屏蔽效应及亲锌层的形成依赖于电解液添加剂,但其有效性取决于这些阳离子或溶剂在锌沉积层或电极表面的吸附行为;因此,观察到的性能提升源于电解液种类与电极界面之间的协同作用,而非仅由电解液的整体性质决定。
3.5溶剂化结构与界面电化学的相互关联
首先,溶剂化结构直接决定了体相电解液中的离子传输特性。Zn²⁺与主要溶剂化鞘层配体之间的结合强度与空间构型,决定了离子迁移的活化能。强配位性的溶剂化结构会提高Zn²⁺迁移的能量势垒,从而加剧欧姆极化效应并降低VE。
其次,溶剂化结构是沉积电位和界面反应的热力学与动力学基础。Zn²⁺与其配体之间的强相互作用通常会降低Zn²⁺/Zn电对的还原电位;然而,过高的锌还原电位会加剧HER。关键是,界面反应的关键步骤Zn2+的去溶剂化需要由初级溶剂化鞘的稳定性直接决定的能量。富含水且高度协调的溶剂化鞘层(例如经典的[Zn(H2O)]6²⁺配合物)会导致较高的去溶剂化能垒,进而引发较大的成核过电位和缓慢的沉积动力学,最终损害CE。因此,理想的溶剂化结构应能协同促进快速离子迁移、实现低过电位沉积,并形成均匀稳定的界面反应,其典型特征表现为“弱溶剂化但动态配位”或“高熵”。例如,由无有机溶剂构型或多种阴离子(如Cl⁻、Br⁻、SO₄²⁻)之间竞争性配位形成的溶剂化环境,既能保持高离子电导率,又能避免形成过于稳定且动力学反应迟缓的配位结构。
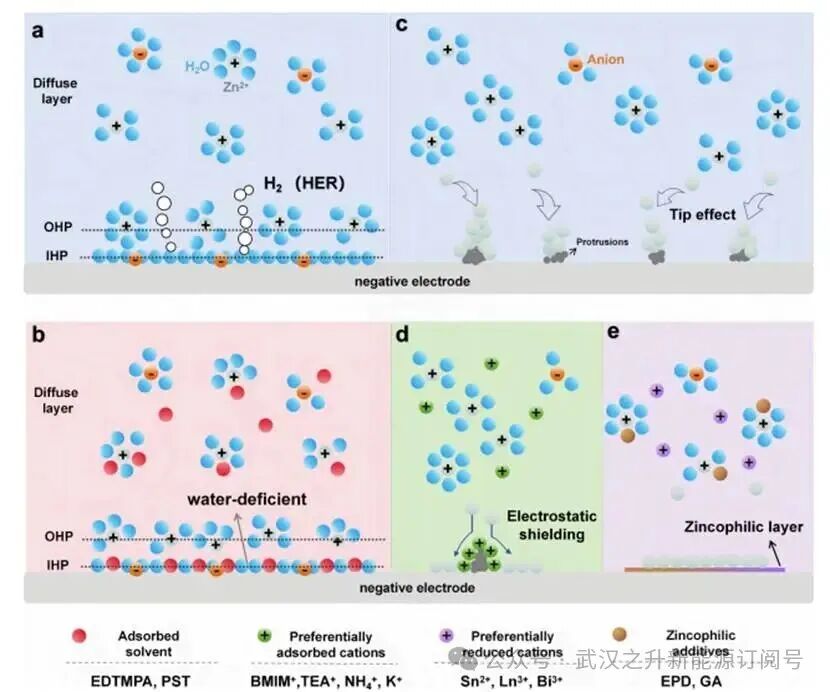
图5锌沉积属于界面电化学过程
3.6卤素反应行为
X⁻氧化为X₂的过程涉及两个X⁻的协同耦合,需要脱溶剂化、克服库仑排斥力以及形成新的X⁻-X键。该过程具有较高的活化能和较小的反应速率常数(图6a)。因此,卤素转化的动力学过程缓慢,导致较高的电化学过电位、较差的倍率容量和有限的功率密度。此外,生成的中性X₂分子具有高度反应活性,会与电解液中丰富的X⁻发生进一步的均相化学反应,形成电化学活性较低的多卤化物阴离子(图6b)。此过程会导致电化学活性X⁻的损失,从而限制电池容量。此外,多卤化物阴离子可溶解于水溶剂中,沿浓度梯度从正极侧穿过隔膜迁移至负极,并与锌沉积发生化学反应(3X₃⁻+2Zn→2Zn²⁺+9X⁻)(图6c)。该过程可能导致CE低下、循环性能较差以及严重的自放电现象。
为解决这些问题,研究重点集中于调控卤素反应途径。涉及提高X2产物的导电性、抑制X−与X2之间的反应,或固定高溶解度的多卤化物。首先,引入强亲核试剂是一种直接且高效的策略。作为路易斯碱,亲核试剂是富含电子且易于攻击缺电子中心的物质。在充电过程中,亲核试剂的关键作用是优先与生成的X2而非X−反应,形成卤素-亲核试剂复合物(X2Nu−或X2−Nu)(图6d)。该方法具有三大优势:(i)由于X2被亲核试剂立即固定,阻止了X2与大量X−的反应,游离活性X−在电解液中保持高浓度,从而提升容量;(ii)形成的卤素-亲核试剂复合物作为新型氧化态载体,其还原能垒通常低于X2的直接还原,可加速卤素反应动力学并提高倍率性能;(iii)通过抑制X−与X2之间的反应阻碍多卤化物生成,有效抑制了穿梭效应。研究表明,SCN−、Cl−和Br−等亲核试剂可分别与I2反应形成I2SCN−、I2Cl−和I2Br−的液态复合物,而聚乙烯醇(PVA)可形成I2−-PVA凝胶复合物,不仅改善了碘转化动力学,还实现了优异的循环稳定性和更高的容量。
与通过亲核策略改变反应路径不同,络合剂的核心作用及电解液阴离子调控机制在于直接作用于已形成的多卤化物,抑制其溶解和迁移(图6e)。络合剂通常采用带有大体积有机阳离子的盐类,例如季铵盐、吡啶鎓盐和咪唑鎓盐。大体积阳离子与多卤化物阴离子之间强烈的静电作用或部分配位作用促进了离子对或配位化合物的形成。这种相互作用降低了系统的吉布斯自由能,从而使生成的络合物在热力学上更加稳定。此外,缓解多卤化物穿梭效应的策略在静态电池与液流电池结构中存在根本性差异:在静态锌卤电池中,固体或凝胶状多卤化物络合物的形成通常是可接受的,因为这些非均相相可被物理限制在阴极结构内部或电极界面处;而在液流电池中,此类异质产物则会带来严重问题,任何沉淀物或粘稠凝胶都可能堵塞多孔电极、阻塞流道并影响泵的运行,导致系统快速失效。
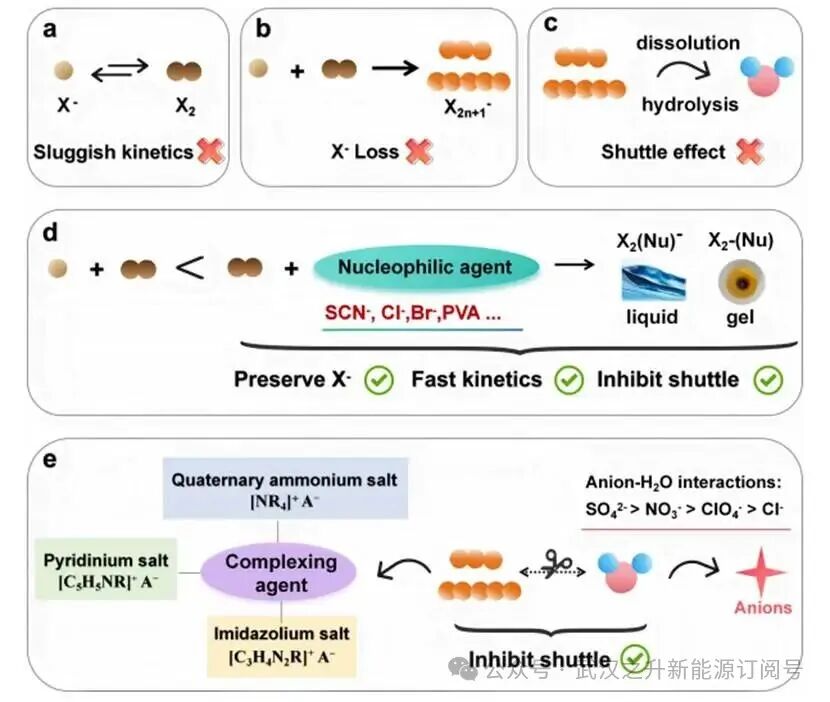
图6.卤素反应行为
3.7.pH调节
电解液pH值通过同时影响卤素氧化还原化学反应及锌电镀/剥离行为,对ZHFBs的循环稳定性起着关键调控作用(图7)。卤素氧化还原对的可逆性高度依赖于电解液的pH,主要与水溶液中卤素离子或元素卤素的化学形态及反应路径相关。在强碱性环境(pH>10)下,所有卤素均会发生两步歧化反应以及可逆反应,因此构建所有卤素氧化还原电对并不实际。此外,所有卤素在水中都会水解。在氯系统中,由于其水解常数最大(K≈7.2×10⁻⁹),氯气在较宽的pH范围内均会发生显著水解。要实现可逆的Cl⁻/Cl2电化学反应,必须采用强酸性介质(pH<2)以使平衡向左移动,从而抑制水解反应。在溴系统中,尽管溴的水解常数(K≈4.2×10⁻⁴)远小于Cl2,但随着pH升高,水解平衡可向右移动。因此,可逆的Br⁻/Br2/Br₃⁻电对实际上仅限于pH<4的范围,以最大限度减少水解损失。在碘系统中,由于水解常数极低(K≈2×10⁻¹³),I₂几乎不发生水解。然而,I⁻/I₂电对的相对较低氧化还原电位(0.54V vs SHE)与O₂/H2O的电位(E°=1.23−0.059×pH,25°C)共同构成了另一限制条件:在酸性介质中,溶解氧对I⁻的氧化反应是自发过程,源于较大的热力学驱动力。因此,可逆I⁻/I₂/I₃⁻反应的最佳操作窗口为接近中性至弱碱性环境(6<<pH<10),以避免酸驱动氧化和碱性歧化反应。因此,三种卤素系统在可逆操作时表现出不同的pH窗口:氯需要强酸性条件(pH<2)以抑制水解;溴需要弱酸性环境(pH<4);而碘在接近中性至弱碱性条件(6<<pH<10)下性能最佳。
锌沉积的形貌和剥离效率受pH环境的调控,因为pH直接影响竞争性副反应的动力学以及表面钝化物种的形成。在强酸性环境中,高H+浓度主导界面反应。其核心机制是HER与锌沉积之间的激烈竞争。从热力学角度看,H+/H2的标准电位(0V vs SHE)远高于Zn2+/Zn的标准电位(−0.76V vs SHE)。然而,在电极表面,H+还原的过电位较高,而Zn2+还原的过电位相对较低,使得锌沉积在动力学上得以发生。尽管如此,电极上高H+浓度的还原过程会消耗电子,从而与Zn2+竞争电荷,导致Zn2+的有效还原电流密度分布不均。此外,H+通过置换反应与锌反应,引发严重的化学腐蚀。HER引起的H2气泡扰动导致Zn2+质量传输不稳定,形成疏松多孔的沉积层,极易产生枝晶。当pH值接近中性时,显著降低的H+浓度会减弱H+的副作用。电荷随后可被高效利用以实现Zn²⁺还原,从而为可逆锌电沉积/剥离创造更有利的热力学和动力学条件。然而,水分解反应带来了新的挑战。生成的OH⁻易与锌离子及阴离子反应,形成电化学惰性的碱性锌盐(如Zn₄SO₄(OH)₆ xH₂O),从而阻碍离子传输。在碱性环境中,锌可直接与OH⁻反应形成Zn(OH)₄²⁻钝化层,抑制后续锌电沉积并增加极化效应。此外,在强碱性条件下,进一步反应会生成无活性的死锌,导致不可逆的容量损失。
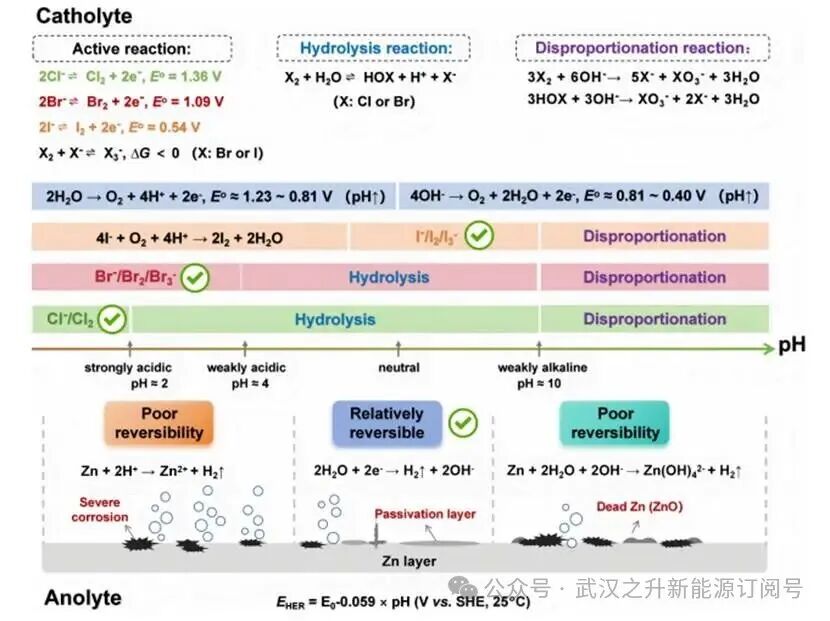
图7.不同pH条件下卤素反应及锌沉积的行为
4.ZCFB的研究
Cl⁻/Cl2(相对于标准氢电极为1.36V)的高电势使ZCFB成为实现超高能量密度的有前景途径,但由于氯的腐蚀性和穿梭效应,应用仍待深入探索(图8a)。基于上述卤素反应机理,未来研究必须超越通用策略:首先,应重点开发具有定制活性位点的析氯反应(CER)催化剂,以最小化氯气的生成能并抑制在高腐蚀性、高电势环境中竞争性的OER;其次,借鉴锌溴或锌碘体系中使用的络合剂,关键方向是设计新型亲核试剂,使其能与氯气形成可逆、稳定且理想情况下不溶于水的络合物,从而从根本上缓解氯气渗透;第三,开发了低活性水作为电解液以抑制氯气溶解度;第四,应采用超选择性、耐氯膜(如先进全氟化或烃基聚合物)及完全密封的负压系统设计,以最大限度降低腐蚀风险和有毒氯暴露风险。
5.卤素的多电子氧化还原途径
卤素的多电子氧化还原路径是突破锌卤素液流电池能量密度限制的关键方向。理想的路径涉及从X⁻依次氧化为X⁰,再进一步氧化为X⁺(甚至更高价态的Xm⁺)(图8b)。然而,核心挑战在于高价态中间体(如I⁺和Br⁺)的热力学不稳定性,中间体易发生水解或歧化反应,导致容量衰减和副反应。在Zn⁻-I液流电池中,构建IBr₂⁻或ICl₂⁻等卤素间物种以稳定I⁺,初步验证了I⁻/I⁰/I⁺四电子转移的可行性。然而,该策略高度依赖高浓度卤化物离子,带来了电解液腐蚀性和成本高昂等问题。在Zn-Br液流电池中,引入溴清除剂可与电生成的溴快速反应,形成稳定的N-溴代氨基磺酸盐(Br-SANa,转移反应),实现Br⁻/Br⁺的稳定化。尽管如此,多电子溴化学仍处于起步阶段。为进一步稳定高价态卤素中间体,未来研究可借鉴静态卤素电池的成功策略,并开发适用于液流体系的电解液工程方案。
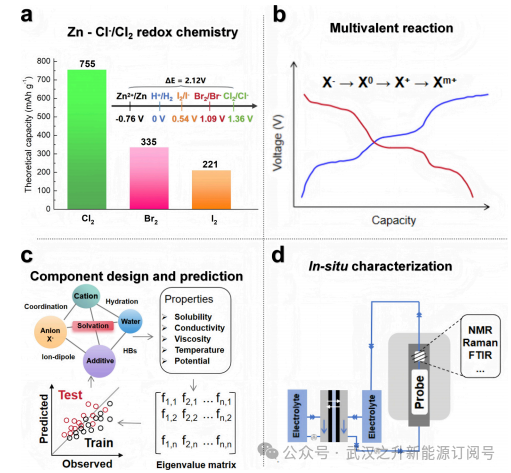
图8.ZHFBs的未来前景
6.电解液预测与逆向设计
要超越低效的试错方法,整合人工智能(AI)、机器学习(ML)和高通量计算技术对于构建用于成分-结构-性能预测的智能平台至关重要(图8c)。这类模型的预测能力从根本上取决于输入数据的质量与相关性,而需涵盖决定材料性能的分子层面相互作用。对于ZHFBs,构建一个基于本综述所讨论机制原理的多维参数空间至关重要。关键描述参数应包括:(i)Zn²⁺与溶剂分子、辅助盐或功能添加剂之间的计算结合能;(ii)基础物理化学参数;(iii)卤素中间体与潜在络合剂之间的相互作用能。
7.原位表征技术用于实时监测动态电解液化学过程
未来研究必须明确探究连续循环、可变流速条件、大容量储能及长期循环如何共同影响溶剂化平衡、卤素物种动力学及组分降解路径。为验证所提出的机制并指导合理设计,实时观测运行条件下的动态电解液化学过程至关重要(图8d)。未来研究应重点整合多种原位技术以深入探究特定ZHFB界面:例如,可运用原位拉曼光谱与FTIR光谱技术监测循环过程中Zn²⁺溶剂化结构及电解液内卤素配合物的动态演变;原位核磁共振光谱技术能实时追踪多卤离子的迁移率、物种分布及交叉现象,为穿梭效应提供直接的定量测量手段。
8.面向实际ZHFB应用的协同优化
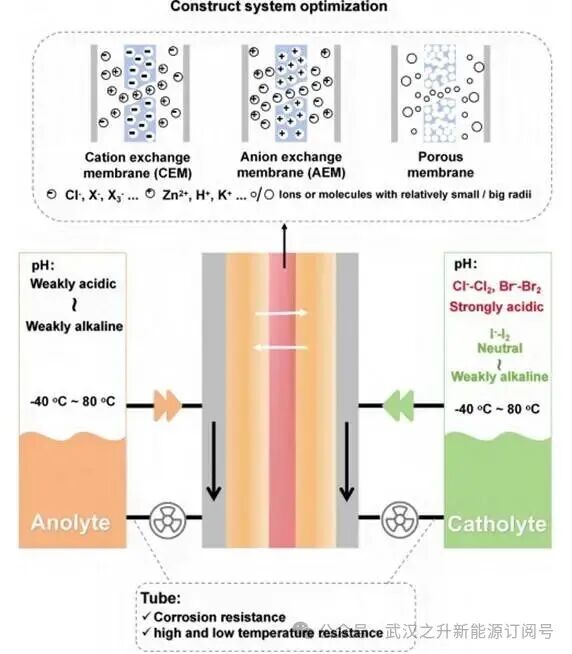
图9.ZHFBs的未来发展前景:面向实际ZHFB应用的协同优化方案
未来的研究应聚焦于一种能够充分考虑这些独特约束条件的协同设计(图9)。协同优化的关键领域包括:
(i)pH值管理。对于可逆的氧化还原反应,pH差异管理至关重要,保持中性/弱碱性阳极电解液以稳定镀锌,同时优化阴极电解液pH以增强卤素反应动力学;
(ii)膜-电解液协同设计。膜的选择都应根据系统的特定离子需求进行定制或组合,以实现最佳的离子选择性和导电性。具有定制孔径的多孔隔膜可能提供最低的电阻,同时有效阻挡大分子复合物;相反,在卤化物化学成分较简单的系统中,可能更倾向于使用CEM或AEM以减少阴离子渗透,但价格相对较高。针对特定电解液组成和流动条件下的离子跨膜传输进行先进的计算建模,对于这种理性的S协同设计至关重要;
(iii)耐腐蚀且宽温度范围的系统架构。卤素的高度反应性要求所有接触部件均采用或涂覆具有卓越化学稳定性的材料。此外,整个系统(包括电解液配方和组件材料)应设计为适用于宽温度范围运行,以确保在各种地理和气候条件下都能保持可靠性能;
(iv)经济性、环境影响及长期稳定性考量:实际部署ZHFB时需解决电解液成本与可持续性问题。附加成本效益必须通过性能提升来证明,而连续循环下的长期稳定性仍然至关重要,但尚未得到充分探索。为降低生态风险,应优先选用环境可生物降解或可回收的络合剂。这些限制因素必须尽早纳入考量,以确保实验室创新成果能够转化为具有商业可行性的技术。