一文学会液流电池的CV与EIS测试
(以全钒液流电池体系为例)
(1)测试简介
在液流电池研究中,循环伏安法(CV)与电化学阻抗谱(EIS)是贯穿电极材料、界面、电解液三大核心体系的通用表征手段,可用来评估电极活性、电解液改性、进行电解液添加剂筛选、电极/电解液的氧化还原反应动力学分析、稳定性判断等研究。具体而言,CV曲线可以快速判断氧化还原反应的可逆性、峰电位、峰电流、反应数量、添加剂对电化学行为的影响;EIS可以解析欧姆阻抗、电荷转移阻抗、扩散阻抗,区分“电极–电解液界面”与 “电解液本体”的贡献,还可以通过Zview等软件进行等效电路拟合,量化不同电阻的贡献。
(2)测试设备
电化学工作站(支持三电极体系),尽量选择允许工作电流较大的,至少要大于2A。
电流等于工作电极电流密度*电极尺寸。
本次演示设备为瑞士万通VIONIC。

接线图示:
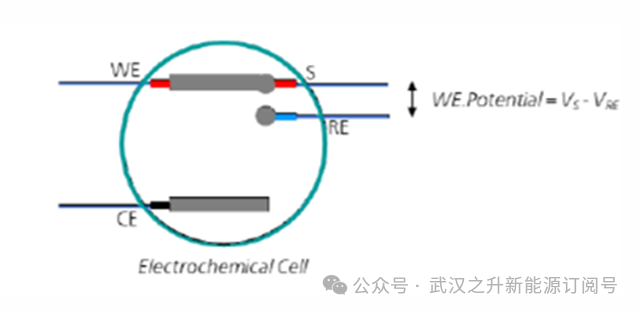
示意图

实物图
(3)测试体系
测试采用三电极体系,不同体系液流电池测试电解液以及电压区间选择都不尽相同,选择原则如下:电压窗口根据半反应的热力学电位确定;参比电极和对电极根据溶液体系以及酸碱性确定。电解液根据其正极侧和负极侧发生的氧化还原反应选择。
如锌溴液流电池正极发生Br⁻/Br₂氧化/还原反应,电压窗口0.5V~1.2V(vs.Ag/AgCl),负极发生Zn²⁺/Zn沉积/溶解反应,电压窗口-1.2V ~ 0V(vs.Ag/AgCl),参比电极可以用Ag/AgCl电极,对电极为铂片。CV和EIS测试时正负极都用0.1M ZnBr2溶液。
如铁铬液流电池正极侧反应为Fe3+/Fe2+,测试电解液一般为0.1 M FeCl2+1 M HCl溶液,电压窗口为0.4V~0.9V(vs.Ag/AgCl),负极反应为Cr3+/Cr2+,测试电解液一般为0.1 M CrCl3+ 1 M HCl溶液,电压窗口为-0.8V~ -0.1V(vs.Ag/AgCl)。对电极为铂片。
使用其他参比电极时可以根据标准氢电极进行电位窗口换算。
(4)实操测试演示(基于全钒液流电池体系)
正极侧VO2+/VO2+:
电解液一般为50-100mL的0.1M VO2++3M H2SO4溶液。
对电极:一般为铂片电极,有时也可以选用碳棒。有条件可以选择大的铂网电极(对电极面积通常是工作电极的10倍以上,从而保证极化只发生在工作电极上),本次测试所用对电极为10×10 cm铂网电极。
工作电极:石墨毡,碳毡,玻碳电极等,本次测试所用为2*2cm石墨毡(XGL)。
参比电极:酸性条件一般用Ag/AgCl电极 也可以用SCE电极。
正极测试CV电位区间一般为0.5-1.4V。
负极侧V2+/V3+:
电解液一般为50-100mL 0.1M V2+ +3M H2SO4溶液,值得注意的是,V2+在空气中极易氧化不能直接配制。本文展示所用电解液为武汉之升新能源提供的3.5价钒电解液通过单电池完全充电后(50-80mA/cm-2先恒流后恒压充电)得到的负极电解液稀释成目标浓度。有条件可以使用全密封电解池并在测试前和测试中通氮气保护。达不到该条件可以取出电解液后迅速测试,现配现用,短时间测试影响较小。
除电解液外,三电极体系其他材料与VO2+/VO2+完全相同。
负极测试CV电位区间一般为-0.8~-0.2V。
第一部分:CV测试
数据处理:
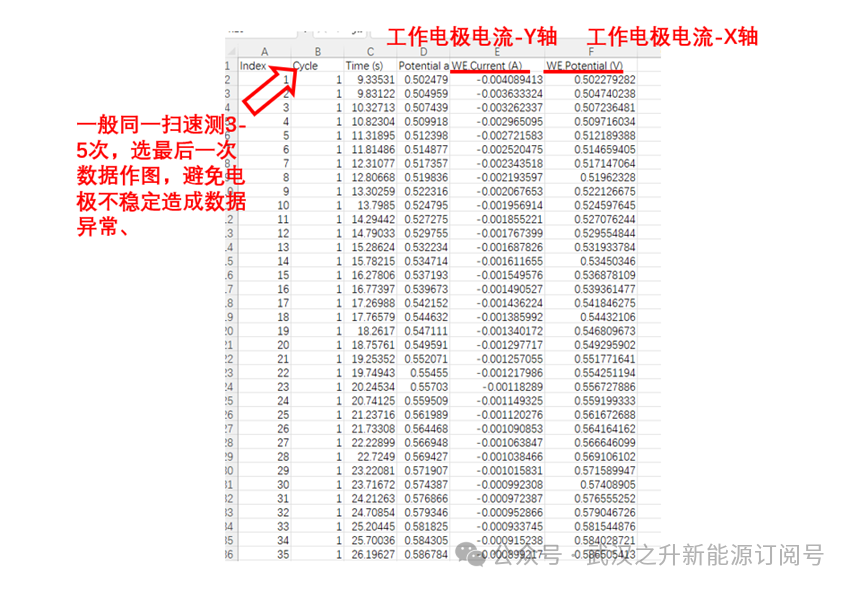
数据展示:
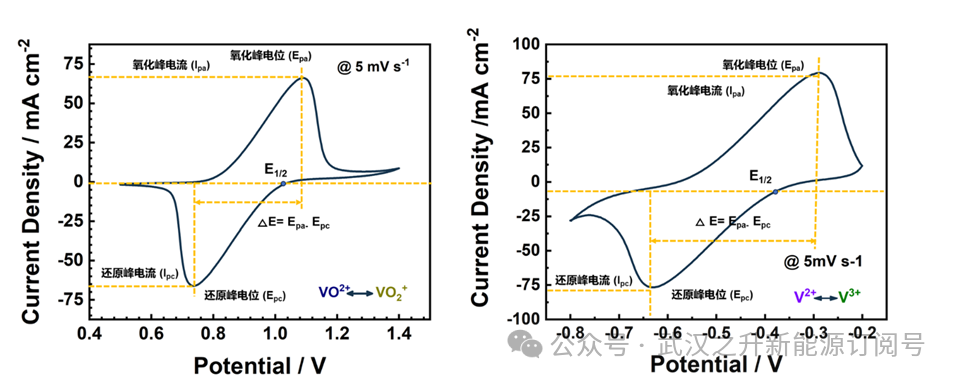
左图为正极电解液,右图为负极电解液
注意:CV测试时,未经改性的原始电极一般在负极电解液中会剧烈析氢,导致没有氧化还原峰(如下图),这是正常现象,上图中的负极电解液CV曲线测试的是改性后的电极。
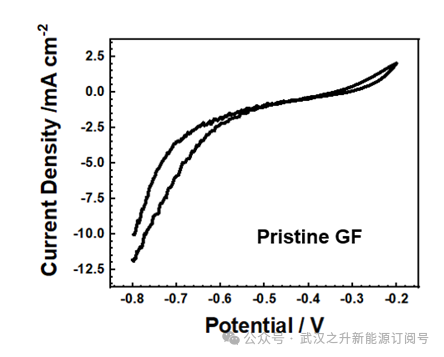
原始电极负极电解液CV测试
CV数据分析:
峰电流(Ip)反映速率和浓度,峰电位(Ep)反映热力学性质,半峰宽:电极有反应可逆性(从峰值电流的一半处画水平线与峰的前沿交点),峰电流比:反应对称性和可逆性。
拓展分析:
低扫描速率下反应受电荷转移速率控制,高扫描速率下反应主要受传质过程控制,不同扫描速率下CV曲线可以有助于获取动力学和热力学参数,有助于深入理解电极反应机理。实际研究中需要根据所关注的特性合理的选择扫描速率。
若反应可逆,还可以根据Randles-Sevcik方程对CV曲线的峰值电流与扫描速率进行定量分析,可以分析反应是否受扩散控制及计算扩散系数。具体而言,若CV峰值与扫描速率二次方根成线性关系,则反应受扩散控制。
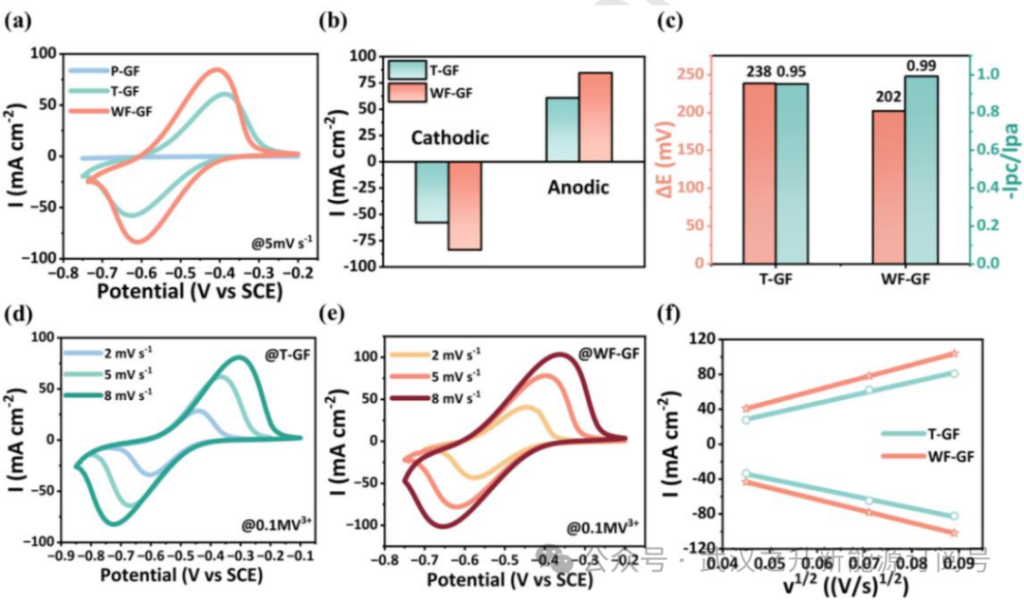
数据来源:【液流论文】天津大学蒋浩然&华北理工大学何章兴CEJ:钒氧化还原液流电池的界面功函数工程设计
第二部分:EIS测试
EIS(电化学阻抗)是通过小振幅交流信号扰动的电化学测量方法,通过分析体系对不同频率交流信号的响应特性,揭示电化学系统的界面结构与反应动力学信息,EIS与CV测试体系,接线方式完全相同,一般测试OCP下,0.01Hz~100kHz,截止电压为5mV/10mV的阻抗谱。
数据处理:
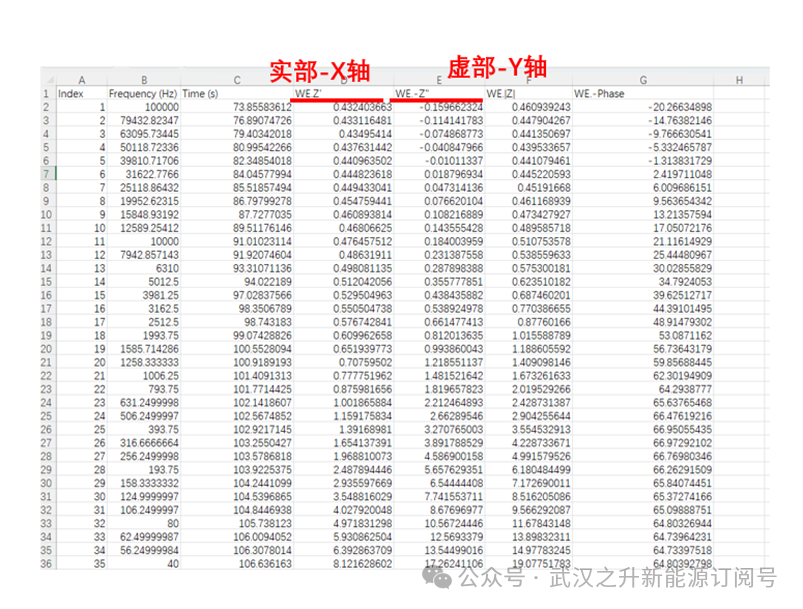
数据展示:
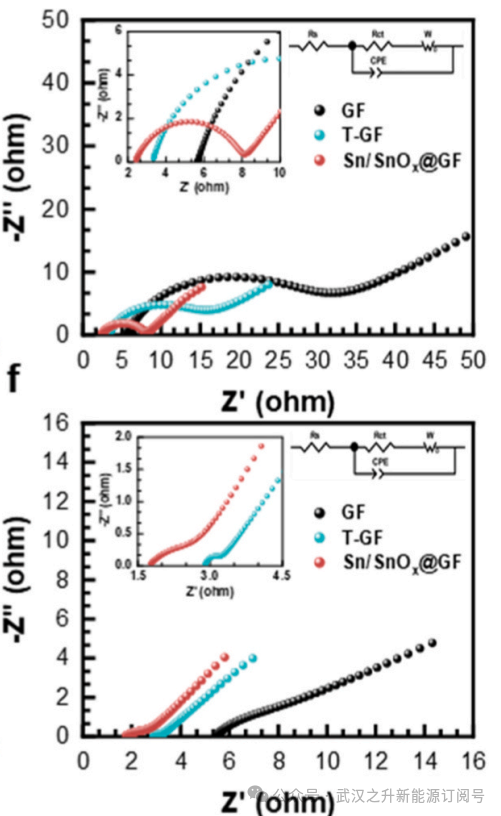
数据来源:【用户论文】祝贺我司用户中石油卢春喜&中石化大连院发表MTC:石墨毡上Sn-SnOx异质结的协同催化作用增强铁铬液流电池中铬的反应动力学
EIS数据分析:
简单来说,EIS图谱解析时一般将总电阻拆解为欧姆电阻、电荷转移电阻和扩散电阻,分别对应电池的三个主要损耗来源。
高频区(>10⁴ Hz),曲线与实轴的交点为等效串联电阻(Rs),对应电解液+隔膜+电极体相的欧姆电阻。Rs越小,意味着离子在电解液和隔膜中的传输阻力越小。
中高频区(1-104Hz)的半圆,为电荷转移电阻(Rct),对应电化学反应的电荷转移过程,Rct越小,说明反应动力学越快,活化极化越小。
低频区 (<1 Hz)的直线,为Warburg阻抗(W),对应活性物质在电极孔隙中的扩散过程,W的斜率越小(越接近45°线),扩散阻力越大。
EIS分析:
EIS读图可以定性分析Rs、Rct和W阻抗的大小。实际分析中,往往通过等效电路图拟合(如用Zview软件等)进行分析。如上图中的散点为EIS实测数据,线图为EIS拟合曲线,拟合电路图以及拟合数据如下:

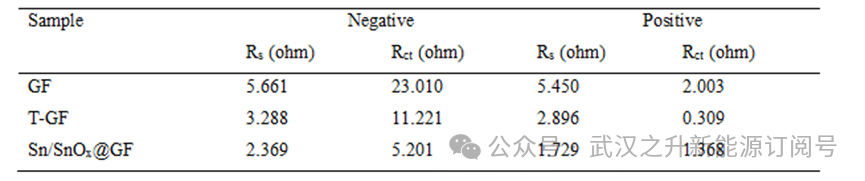
其中,CPE为常相位角元件,对应电极/电解质界面的双电层电容行为。
此外,EIS还可以进行DRT(Distribution of Relaxation Times,弛豫时间分布)进阶分析。传统的Nyquist图中,时间常数相近的过程(如嵌入和析氢反应)会重叠在一起,难以区分。而DRT通过数学变换将EIS数据分解到时间常数维度,可在时域中分离这些重叠的过程。DRT通过将EIS数据解卷积到各过程的时间常数来处理这个问题,从而避免了寻找合适等效电路模型的必要性,无需先验知识即可进行数据评估。
(5)总结
CV和EIS分析是电化学行为中的基础也是重要分析手段,二者可以提供大量有效信息,帮助研究者快速定性定量判断电极改性,电解液添加等相比于原始/商用电极,电解液,催化剂等的优劣。准确的测试是科研顺利的先决条件,祝大家测试顺利,科研顺利!